科室新闻
成果发表丨陈革&张鸿祺教授团队:通过单细胞测序联合空间转录组测序确定釉质细胞型颅咽管瘤治疗新靶点
2024年6月,首都医科大学宣武医院神经外科陈革&张鸿祺教授团队在《Cancer Letters》(JCR分区Q1,IF:9.7)期刊上发表了题为“Axl as a potential therapeutic target for adamantinomatous craniopharyngiomas: Based on single nucleus RNA-seq and spatial transcriptome profiling”的研究论文。宣武医院神经外科陈奕光博士、刘小海副主任医师为共同第一作者,陈革教授、张鸿祺教授为通讯作者。

颅咽管瘤是一种罕见的良性鞍区上皮肿瘤,起源于胚胎时期rathke囊残余组织。发病高峰期在5-15岁以及40-55岁左右,呈双峰状。目前,首次手术全切除是现在颅咽管瘤的主要根治手段。但因为手术复杂和肿瘤黏连的特点导致切除不完全的患者可能会出现术后复发,而过于激进地对部分患者(例如与下丘脑黏连紧密者)进行全切除或对复发患者进行多次手术也容易导致严重的下丘脑-垂体内分泌功能障碍,严重影响生活质量。陈革&张鸿祺教授团队此前2023年9月发表在《Neurosurgical Review》的颅咽管瘤临床回顾性研究“Impact of three surgical approaches on the therapeutic efficacy of intraventricular craniopharyngiomas: a single-center retrospective analysis”(JCR分区Q1),结果也提示手术切除率的提高往往伴随着更高的术后垂体功能障碍发生的风险。因此,目前亟需有效的治疗手段来减少复发和术后并发症。
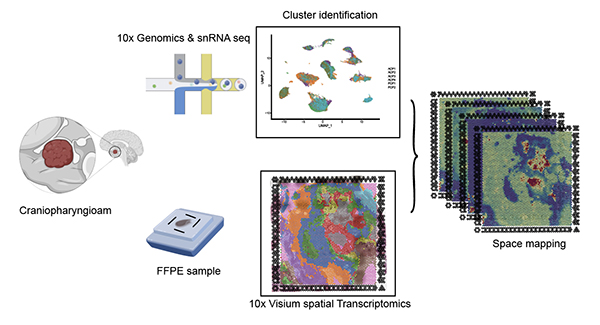
图1 单细胞测序联合空间转录组测序分析颅咽管瘤微环境
本次研究,陈革教授团队通过收集临床患者的肿瘤样本组织进行单细胞测序和空间转录组测序,通过分析颅咽管瘤患者的肿瘤异质性和基因空间表达分布情况来寻找颅咽管瘤治疗的潜在靶点。
首先,团队对6例颅咽管瘤组织样品进行单细胞测序(包括4例釉质型颅咽管瘤及2例鳞状乳头型颅咽管瘤),以及1例釉质型颅咽管瘤进行空间转录组测序。检测发现肿瘤样本中异质性高,肿瘤组织中上皮细胞成分复杂。在肿瘤细胞方面,釉质型肿瘤样本和鳞状乳头型肿瘤样本存在较为明显差异,其中釉质型肿瘤样本特异性存在丰富的EDAR+/LEF1+的细胞群,经空间转录组映射分析发现,该细胞群与釉质细胞型颅咽管瘤中特异性存在涡轮样细胞的空间定位高度重合,并通过免疫荧光实验进一步证实了这些表达模式。
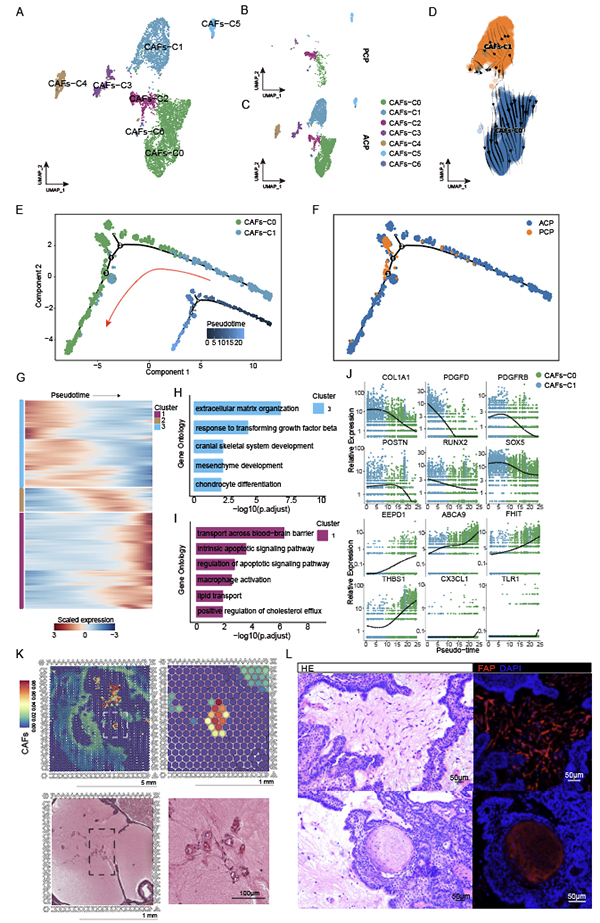
图2 CAFs亚群分析&拟时序分析
另外,数据中存在较为丰富的FAP+肿瘤相关成纤维细胞群(Cancer-Associated Fibroblasts,CAFs),这在恶性肿瘤中被广泛报道,且具有免疫抑制和促进肿瘤恶性进程的功能,但在颅咽管瘤中并没有被详细报道。因此,团队利用空转映射定位和免疫荧光确定了CAFs在釉质型颅咽管瘤间质中丰富表达,并且呈现明显的纤维细胞状外观。接着利用亚群分析和拟时序分析对CAFs进行全面分析,发现大部分FAP+CAFs细胞在釉质型颅咽管瘤中富集,该部分细胞呈现“钙化/软骨化-胆固醇外排/凋亡”的方向进行分化;最后通过免疫组化实验在胆固醇结晶和钙化/湿性角化物交界区域证实了大量CAFs的存在,因此釉质型颅咽管瘤中的钙化及胆固醇结晶的形成可能与CAFs的分化相关。
为了进一步探究CAFs与釉质型颅咽管瘤潜在的相互作用关系,团队利用细胞间通讯分析发现PROS1/GAS6-AXL在CAFs与肿瘤上皮细胞间信号传导高表达。利用多重免疫荧光发现,AXL受体主要表达在肿瘤上皮细胞中,而PROS1配体主要表达在囊腔和湿性角化物中,GAS6配体主要表达在钙化灶中,并且上述配体和FAP+CAFs存在共定位表达,因此我们推断CAFs分化形成钙化/湿性角化物的过程中分泌PROS1及GAS6配体作用于周围的肿瘤上皮细胞激活AXL受体。此前有研究提示PD-L1在釉质型颅咽管瘤的基底样上皮细胞中表达。团队利用免疫荧光发现PD-L1与AXL也存在共定位表达,提示AXL受体的激活可能促进肿瘤的免疫抑制,从而推动肿瘤的发生发展。
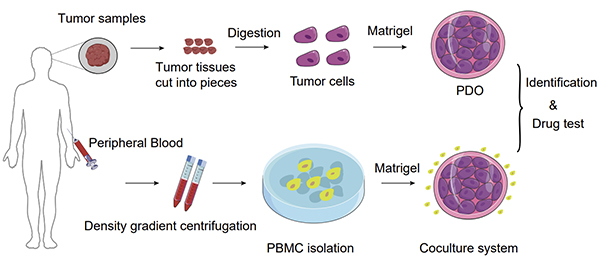
图3 PDO构建&免疫共培养模型构建
为了证实上述假设,团队通过收集釉质型颅咽管瘤临床组织样本,成功构建了8例PDO类器官模型(Patient Drived Organoid),并且利用其中4例构建PBMC(Peripheral blood mononuclear cell)免疫共培养类器官模型。随后,在8例类器官中外源性添加Bemcentinib(AXL选择性小分子靶向药),经计算测得药物IC50值约为1.697uM。观察96h后药物杀伤效果,发现类器官组织团块的直径和活力都较对照组明显下降,并且呈浓度依赖性。另外将Bemcentinib与PD-L1抑制剂(Atezolizumab)联合作用于免疫共培养类器官模型中发现,联合组的抑制效果比单纯使用PD-L1抑制剂的效果要更优,说明阻断AXL的活性可以增强免疫治疗的效果。
釉质型颅咽管瘤类器官生长形态变化
为了探究AXL和PD-L1之间的调控关系,团队通过western blot实验发现:Bemcentinib处理组中的类器官p-AXL和PD-L1的蛋白表达明显受到抑制,而外源性添加GAS6刺激类器官后p-AXL和PD-L1的蛋白表达明显上调,并且可以抵消Bemcentinib的抑制作用。接着团队通过对釉质型颅咽管瘤的新鲜组织进行蛋白提取和Co-IP实验,发现肿瘤中PD-L1和AXL存在互作关系。因此釉质型颅咽管瘤中通过激活GAS6/AXL/PD-L1信号通路促进肿瘤的免疫抑制和进展。
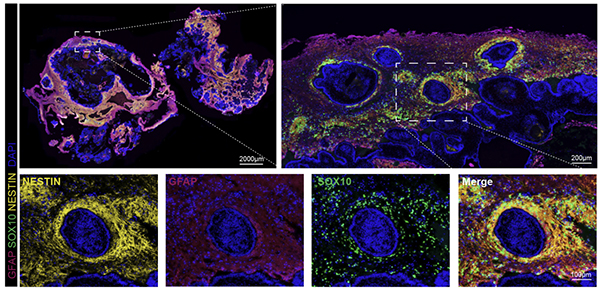
图4 颅咽管瘤指状突起结构周围存在神经嵴样细胞
最后,团队通过空间转录组数据对肿瘤周围的胶质反应带进行拟时序分析,发现靠近肿瘤一侧特别是指状突起结构附近的胶质细胞具有神经干细胞的特点。通过多重免疫荧光验证该群细胞可能具有神经嵴样细胞的特点。
本研究的主要目的是探究釉质型颅咽管瘤微环境中潜在的治疗靶点。我们的结果提示,AXL可以作为未来颅咽管瘤靶向治疗的可靠靶点,并且AXL抑制剂Bemcentinib在类器官水平上可以有效增强Atezolizumab免疫治疗的效果。
论文链接:
https://doi.org/10.1016/j.canlet.2024.216905

通讯作者
陈革,首都医科大学宣武医院神经外科,主任医师、教授、硕士生导师。1992年毕业于首都医科大学,在首都医科大学宣武医院神经外科工作至今。2001年10月至2002年4月到德国美茵茨(Mainz)大学附属医院神经外科学习,跟随世界著名微创神经外科大师Axel Perneczky教授学习微侵袭神经外科,观摩大量微创手术并在德国图特林根参加一期内镜颅底解剖培训班。期间到奥地利维也纳大学解剖学院跟随世界著名内镜解剖大师Manfred Tschabitscher教授学习内镜和显微神经解剖。回国后在宣武医院率先开展了神经内镜微创手术,是国内最早开展神经内镜微创手术的医生之一。2005年3月至5月到日本东京慈惠大学附属医院神经外科访问研究,跟随大井静雄(Shizuo Oi)教授从事训练用内镜下经鼻蝶入路颅底模型的试验研究。目前已完成各种类型垂体肿瘤1300例以上,在各种颅底肿瘤包括颅咽管瘤、脑膜瘤、脊索瘤、听神经瘤及面肌痉挛和三叉神经痛的治疗方面积累了丰富的经验。目前作为主要研究者参加替莫唑胺联合放疗难治性垂体瘤前瞻性多中心临床研究
【出诊时间】周一上午(专家门诊)、周三上午(特需门诊)

通讯作者
张鸿祺,首都医科大学宣武医院神经外科,主任医师、教授、博士生导师,现任首都医科大学宣武医院神经外科主任。目前担任世界介入神经放射联合会(WFITN)执行委员,亚洲及大洋洲介入神经放射联合会(AAFITN)执行委员、中国医师协会神经介入专业委员会主任委员、中华医学会神经外科学分会常委,中国老年学学会心脑血管病专业委员会常务理事、北京医学会神经外科分会副主委、《中国脑血管病杂志》《中国微侵袭神经外科杂志》编委、《JNIS》中文版主编多年来,一直从事脑与脊髓血管病的外科和介入治疗,在脑动脉瘤、颅脑血管畸形、脊髓血管畸形等方面的临床和研究工作处于国内外领先水平。承担及完成“十三五”国家重点研发专项、国家自然科学基金项目等各级科研课题20项,在《JAMA Neurology》《BRAIN》《Annals of Neurology》等学术期刊发表论著170余篇,曾获国家科技进步二等奖。
【出诊时间】周二晚(特需门诊)

共同第一作者
陈奕光,首都医科大学宣武医院2022级外科学(神经外科)专业型博士研究生,美国Cedars-Sinai Medical Center联合培养博士研究生。主要进行颅咽管瘤及下丘脑功能相关研究。在《Journal of Neuroinflammation》、《Cancer Letters》等学术期刊发表SCI文章6篇。获得国家发明专利1项。

共同第一作者
刘小海,首都医科大学宣武医院神经外科,副主任医师。2009年-2012年于北京协和医院神经外科攻读博士学位,师从王任直教授。2012年7月-2019年6月于协和医院神经外科工作,期间2013年3月至2015年12月于美国 Cedars-Sinai Medical Center进行垂体腺瘤方面的博士后研究。2019年6月调入宣武医院神经外科工作,主要从事垂体瘤、颅咽管瘤、脊索瘤等颅底肿瘤诊疗工作。《中国难治性垂体腺瘤专家诊治共识(2019)》执笔人之一及编委,《中国复发性垂体腺瘤专家诊治共识(2019)》《中国垂体促甲状腺激素腺瘤诊治专家共识(2017)》《中国库欣病诊治专家共识(2015)》编委,以第一(共同)或通讯作者发表垂体瘤颅咽管瘤脊索瘤相关SCI论文20余篇,主持国家自然科学基金青年项目、首都卫生发展基金“青年优才”基金及”自主创新“基金,入选北京市医管局“青苗”计划、“培育”计划等多项课题。科研成果曾获教育部科学技术进步奖二等奖(排名第3)。
【出诊时间】周一上午、周三下午(专科门诊)





















